
非酒精性脂肪肝炎(Nonalcoholic Steatohepatitis,NASH)是非酒精性脂肪性肝病(Nonalcoholic Fatty Liver Disease,NAFLD)疾病谱中的进展形式,是脂质在肝组织内累积造成肝脏损伤和炎症。NASH患者若不及时治疗,可能进一步发展成肝纤维化、肝硬化甚至原发性肝癌,严重威胁人类健康。有专家预测,至2025年,全球NASH的治疗市场规模将达到150亿美元。但是截止2024年3月14日,仅有一款药物(商品名为Rezdiffra,THR-β激动剂)被美国FDA批准用于NASH的治疗,治疗NASH的有效药物仍十分缺乏。因此,探索NASH的有效治疗药物具有广阔的市场空间和巨大的社会价值。
法尼醇X受体(farnesoid X receptor, FXR)是核受体超家族的一员,主要广泛分布于肝脏、肠道、肾脏、胆囊等器官。FXR作为一种代谢的调节因子,在胆汁酸、胆固醇、脂质以及葡萄糖代谢中发挥着重要的作用,被认为是治疗NASH非常有潜力的靶点。近期研究表明,FXR拮抗剂,尤其是肠道选择性的FXR拮抗,对高脂饮食诱导NASH小鼠的肝脏脂肪变性、肝炎和肝纤维化展现出明显的缓解效果。目前FXR拮抗剂的研究相对于FXR激动剂而言相对落后,具有较大的开发前景。大部分FXR拮抗剂都是天然产物,如Gugggulsterone,甘氨熊去氧胆酸(GUDCA)和牛磺熊去氧胆酸(TUDCA)等,且目前仅有一款FXR拮抗剂进入临床,是由上海医工院和江苏柯菲平联合开发的SIPI-7623,处于临床一期,适应症为混合型高血脂。因此,FXR拮抗剂的研究也渐渐成为了研究热点,研发结构新颖的FXR拮抗剂用于治疗NASH具有重大的意义。
近期,桂林医学院药学院谭相端博士团队和桂林医学院公共卫生学院余启明博士团队在抗NASH药物研究领域取得新进展,于药物化学权威期刊European Journal of Medicinal Chemistry (药物化学1区, IF=6.7) 发表题为“Discovery of 4-aminophenylacetamide derivatives as intestine-specific farnesoid X receptor antagonists for the potential treatment of nonalcoholic steatohepatitis”的研究性论文, 文章中报道了一类结构新颖的4-氨基苯乙酰胺骨架化合物为肠道选择性FXR拮抗剂,并用于抗NASH研究(图1)。
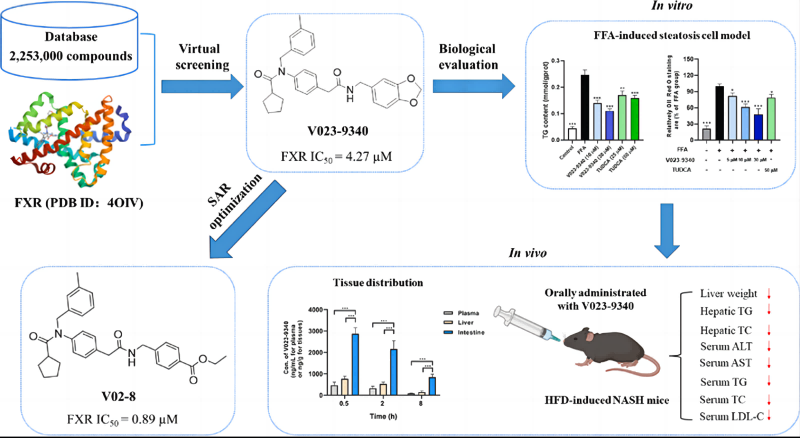
图1:文章内容摘要
一、虚拟筛选
首先,作者根据FXR与报道的FXR拮抗剂NDB的蛋白晶体复合物(PDB ID: 4OIV)分别建立了药效团、三种分子对接模型。从ChemDiv、Life chemicals、DrugBank数据库中下载了2,253,000个化合物,并进行类药性筛选(Lipinski rule of five and Veber rules)得到2,203,000个成药性类药性较好的小分子。然后,对化合物依次进行药效团筛选(Fit value > 2.5)、Libdock分子对接筛选(Libdockscore > 130)、CDOCKER分子对接筛选(-CDOCKER interaction energy > 50 kcal/mol)、Autodock Vina 分子对接筛选(Autodock Vina affinity < -8 kcal/mol),得到200个与蛋白FXR预测结合强度高的苗头化合物。选取其中预测结合强度高于阳性化合物NDB、TUDCA,且结构骨架不同的35个化合物进行购买并用于后续研究(图2)。
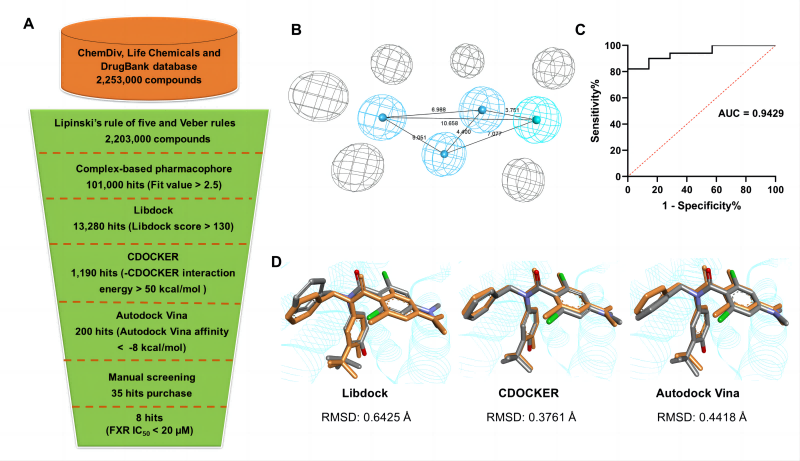
图2: 虚拟筛选流程
二、体外FXR拮抗活性筛选
作者使用细胞水平的双荧光素酶报告基因检测法,在体外筛选化合物对FXR的拮抗活性。如图3中显示,35个化合物都显示出了一定的FXR拮抗活性。其中,8个化合物(V023-9340, V006-7855、 V008-3857、V022-1200、V024-5097、V006-8858、V009-0933、V026-7567)的拮抗活性明显强于阳性化合物TUDCA、GS。其中拥有4-氨基苯乙酰胺类骨架的化合物V023-9340显示出最强效的FXR拮抗活性,因此,作者选择V023-9340进行后续更加深入的生物活性研究。
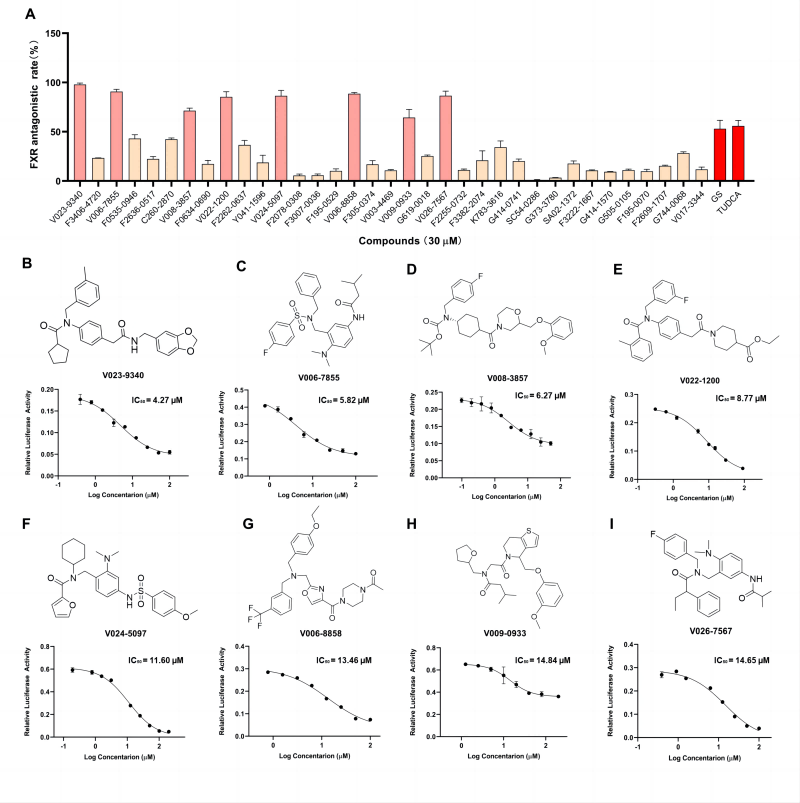
图3: 体外FXR拮抗活性筛选
三、化合物V023-9340体外改善细胞脂肪变性效果
为测试V023-9340的体外改善细胞脂肪变性的活性,作者在体外使用游离脂肪酸构建了细胞脂质堆积模型,并用V023-9340处理24 h,观察细胞的脂质含量变化。由图4可以看到,V023-9340可剂量依赖性改善细胞的脂质堆积,具有很好的改善细胞脂肪变性效果。
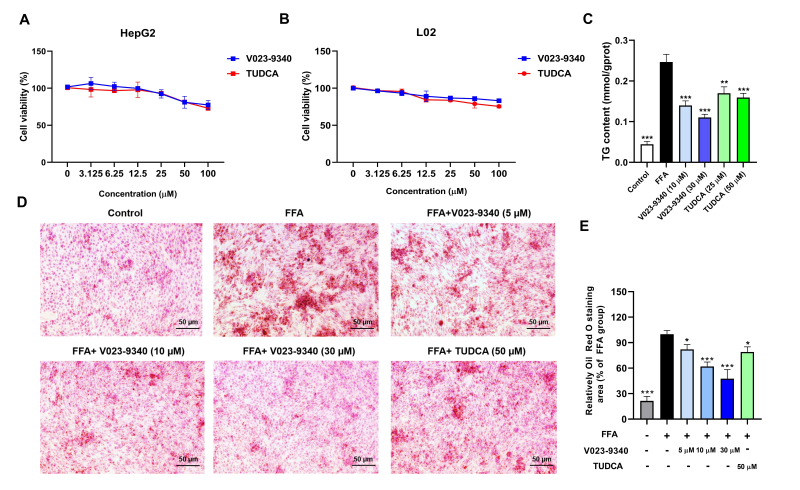
图4: 体外改善细胞脂肪变性活性研究
四、化合物V023-9340对高脂饮食诱导的NASH小鼠的改善作用
在组织分布研究中,V023-9340口服后可以显著聚集于肠道,在肠道的浓度远大于肝脏、血浆,证明了其为潜在的肠道FXR拮抗剂。进一步,作者将V023-9340用于高脂饮食诱导的NASH小鼠中,验证其对NASH的缓解效果(图5)。V023-9340可以显著降低NASH模型小鼠的体脂含量,缓解了肥胖的症状。另外,肝重、肝脏甘油三酯含量、肝脏总胆固醇含量也明显降低。血清中的AST、ALT含量也剂量依赖性减少,表示了V023-9340对肝损伤的保护作用。组织切片结果显示V023-9340可缓解NASH小鼠肝脏的脂肪变性、炎症,对肝脏纤维化也有一定的缓解效果。另外,V023-9340还可以缓解了NASH小鼠的血脂异常,降低了血清中的TG、TC、LDL含量,但对HDL没有明显的影响效果。

图5: 体内抗NASH活性研究
五、化合物V023-9340对高脂饮食诱导的NASH小鼠的作用机制研究
为更好的阐释V023-9340在体内的作用机制,作者使用qRT-PCR实验测试组织中mRNA的表达差异情况(图6)。结果显示,V023-9340剂量依赖性地降低了回肠中Fxr基因表达,并调控了其下游靶基因。肝脏中,Fxr基因表达并没有下降,反而有在20 mg/kg下有一定的上升。Westen blot实验进一步验证了肝脏中FXR、SHP、CYP7A1的蛋白表达情况。另外,V023-9340也降低了肝脏中的炎症因子Tnf-α、IL-1β、以及纤维化相关基因Col1a1、脂质代谢相关因子Cd36、Acsl1等的表达。
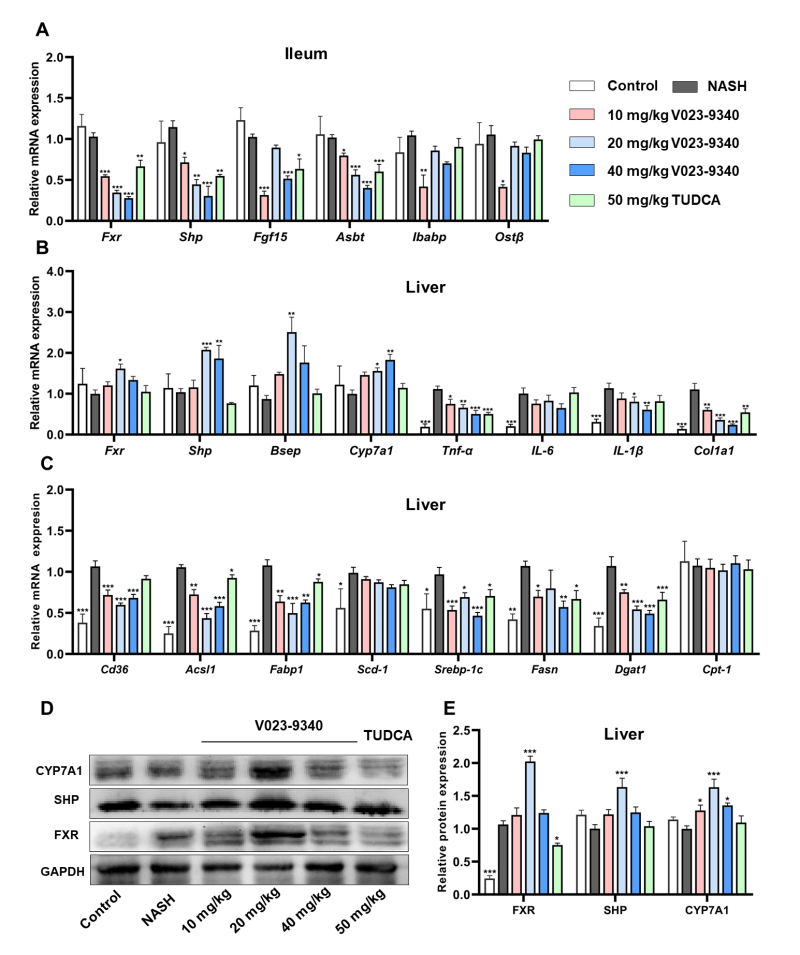
图6: V023-9340机制研究
六、化合物V023-9340的结合模式分析
为了研究 V023-9340 与 FXR 配体结合域(LBD)的结合分子机制并指导进一步的结构优化,作者进行了分子对接分析和分子动力学模拟(MD)研究(图7)。结果表明,在 MD 模拟过程中,V023-9340 可与 FXR LBD 稳定结合。此外,还利用分子力学泊松-波尔兹曼表面积(MM-PBSA)算法计算了 MD 模拟轨迹的结合自由能。经计算,NDB-4OIV 和 V023-9340-4OIV 的相对结合自由能分别为 -52.954 kcal/mol 和 -62.298 kcal/mol,V023-9340 与 FXR LBD 结合贡献最高的氨基酸残基分别是 Leu291、Met294、Ala295、Met332、Met369、His451、Ala452 和 Leu455(图 7C)。具体而言,氨基酸 His451 和 Met369 与 V023-9340 的环戊基形成疏水相互作用,而氨基酸 Ala295、Met332、Ala452 和 Leu455 与甲基苯基形成疏水相互作用。氨基酸Leu291 通过疏水作用与 V023-9340 的苯基相互作用。
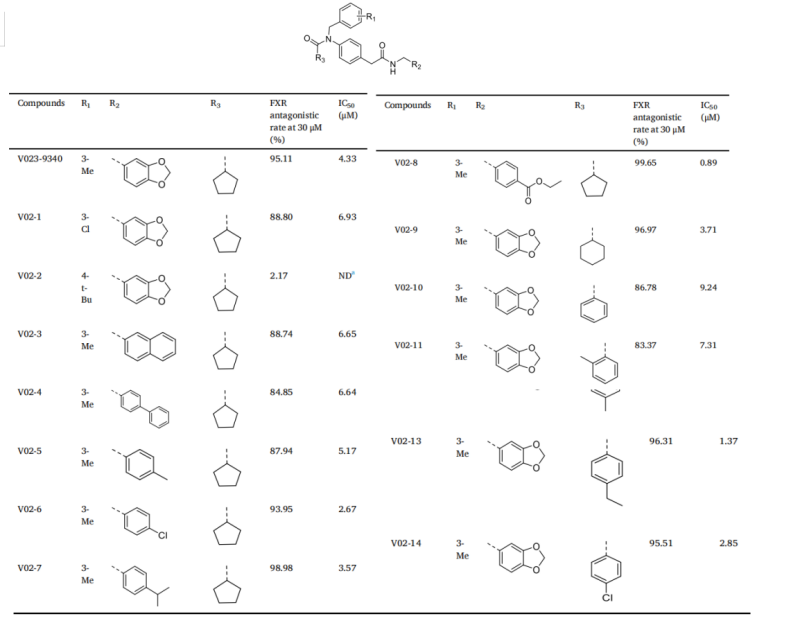
根据上述结合模式分析,作者保留了4-氨基苯乙酰胺骨架,并对V023-9340 的A、B 和 C 三个区分别进行了修改,以初步研究其构效关系(表1)。结果发现,B、C区域引入疏水性基团都可以在一定程度上增强对FXR的拮抗活性。特别是在B区域中将1,3-苯并间二氧杂环戊烯换成苯甲酸乙酯基团后,化合物的FXR拮抗活性明显提高,IC50达到0.89 µM。
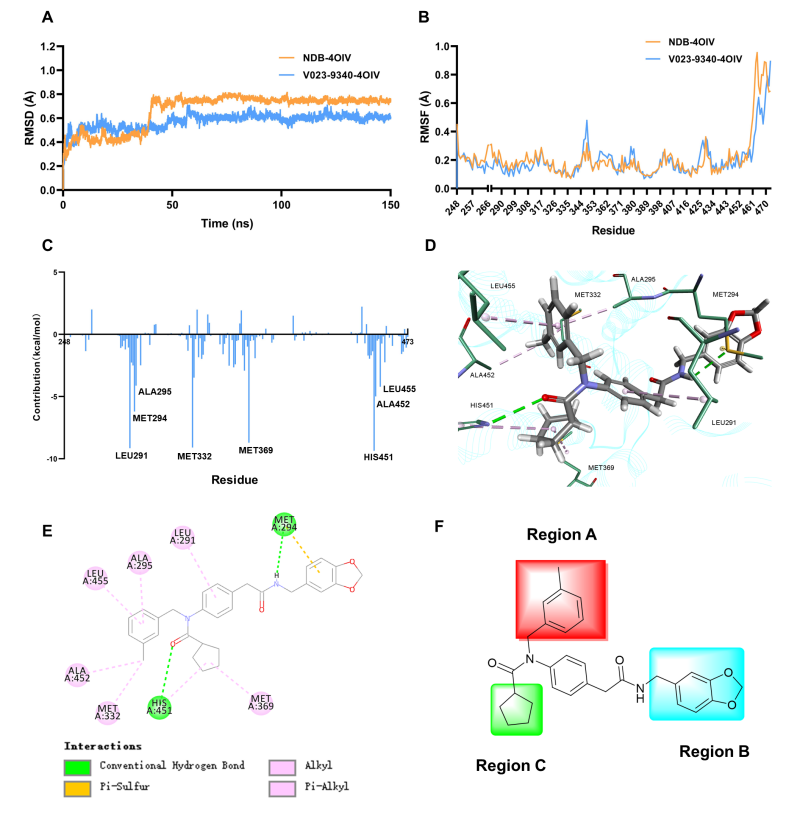
图7: 分子模拟研究
表1:V023-9340 的SAR研究
结论:
1. 作者根据虚拟筛选与体外活性筛选,成功筛选出多个结构、骨架新颖的新型FXR拮抗剂,其中8个化合物的FXR IC50都小于20 µM,扩大了现有的FXR拮抗剂的骨架类型。
2. 发现4-氨基苯乙酰胺类化合物V023-9340为新型肠道FXR拮抗剂,在高脂饮食诱导的NASH小鼠中,明显缓解了小鼠肝脏的脂肪变性、炎症,可作为抗NASH的先导化合物。
3. 根据合理药物设计,对4-氨基苯乙酰胺类化合物V023-9340进行构效关系研究,设计并合成出衍生物V02-8,拮抗FXR的 IC50达到0.89 µM。
参考文献
Cong Chen, Bing Zhang, Jiaojiao Tu, Yanfen Peng, Yihuan Zhou, Xinping Yang, Qiming Yu, Xiangduan Tan,Discovery of 4-aminophenylacetamide derivatives as intestine-specific farnesoid X receptor antagonists for the potential treatment of nonalcoholic steatohepatitis,European Journal of Medicinal Chemistry,Volume 264,
2024,115992,https://doi.org/10.1016/j.ejmech.2023.115992.
致谢
本文由文章一作作者桂林医学院谭相端老师在读研究生陈聪投稿,再此表示感谢!



