前言
AI赋能小分子化合物逆合成路线设计软件SYNTHIA™(原名Chematica)的研发团队,来自波兰科学院有机所和韩国蔚山国立科学技术研究所 (UNIST) 的Bartosz Grzybowski教授与美国西北大学的Milan Mrksich教授以及Merck旗下的美国MilliporeSigma公司的研发人员合作,使用SYNTHIA™在实验室进行了一场实战演练。他们选择了6个具有生物活性的分子、1个重磅药物(赛诺菲▪安万特制药公司开发的抗心律失常药物Dronedarone)和1个天然产物(Engelheptanoxide C)作为目标物,而SYNTHIA™在3个小时内便提供出所有目标分子的理想合成路线和反应条件。化学家则按照这些合成路线在实验室里进行合成实验,以检验这些路线是否可靠。研究者对每一步反应的条件进行了优化,并且为了增加难度,他们给这场演练设置了一些限制条件,比如要求实验员筛选每步反应条件的次数不得超过5次,最终每个分子的合成总耗时必须控制在70小时以内。结果表明,对于其中的7个目标分子,SYNTHIATM创建的路线不仅与此前化学家报道的合成路线明显不同,而且步骤更少或是产率更高、耗时更短、成本更低。此外,第8个天然产物更是在SYNTHIA™的帮助下实现了首次合成。相关工作发表在Chem【1】 杂志上。
一、关于SYNTHIA™
SYNTHIA™是一款AI赋能小分子化合物逆合成路线设计软件,它由有机化学家联合计算机专家对化学反应的规则和逻辑进行编码,将编码后的反应规则储存在SYNTHIA™的数据库中,历经19年精心设计,该数据库目前已包含10万多种手动编码的反应规则,并且每个季度都在更新。利用SYNTHIA™可以轻松自定义搜索条件,可应用与于复杂化合物、天然产物和全新药物分子的合成路线快速设计;已知化合物的合成工艺路线优化。路线设计时能够考虑到兼顾不兼容基团、基团保护与脱保护、区域和立体选择性、空间位阻和电子效应等因素。SYNTHIA™探索创新和已知的解决方案,排除不可行选择,为用户提供合适的合成路线。

图1:识别化学环境,保护不兼容基团
SYNTHIA™在设计合成路线时,不仅仅只考虑是否满足对应的化学反应规则。如图1所示,对于实际设计的反应路线,除了匹配到对应的反应规则以外,SYNTHIA™还能够识别出反应路线中满足反应规则以外的片段是否是需要保护的片段,是否是该化学反应规则不兼容的片段。对应识别出需要保护的片段,SYNTHIA™会明确指出,而且会提供保护基选择的方案。
SYNTHIA™在设计合成路线时,还会兼顾区域和立体选择性、空间位阻和电子效应等因素。如图2所示,a中手性产物的生成是由于原料片段中空间位阻的存在和合理的电子效应;b中由于硝基的吸电子效应导致反应活性位点发生变化而不能合成目标分子;c中电子效应没有变化,但是空间位阻效应消失使得反应能够正常发生但是不能达成手性合成的目的。
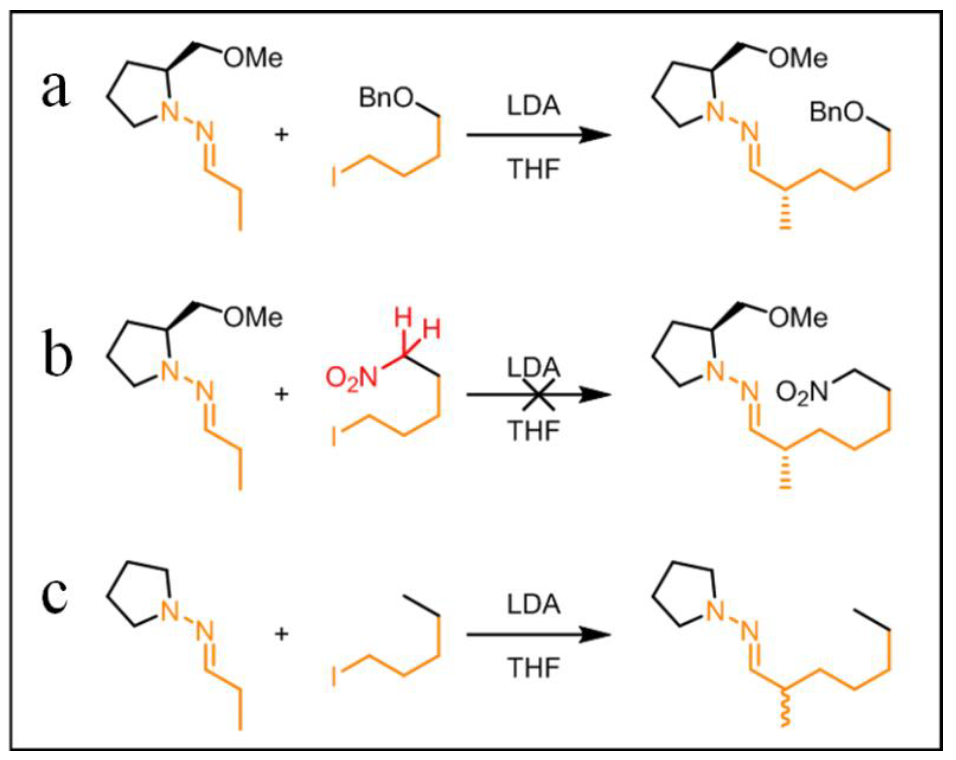
图2:识别空间位阻和电子效应
除了上诉提到的识别化学环境,保护不兼容基团和识别空间位阻和电子效应,SYNTHIA™为了能够像化学家一样思考来设计合成路线,添加了一些策略上的功能,包括通过两步法策略和复杂程度更高的中间体合成目标分子(图3a)、约100个编码的FGI(官能团转换)规则,以快速到达反应性较低的合成子(图3b)、通过旁路算法绕过潜在反应性冲突的程序,将冲突基团转化为非冲突基团(图3c)和多个反应位点在反应条件下具有反应性,则同时对中间体进行两种不同反应的能力(图3d)。

图3:SYNTHIA™中内置的像化学家一样思考的策略
二、实验验证案例
1、已报道化合物BRD7/9 抑制剂合成路线优化
实验测试的靠前化合物是已报道的选择性BRD7/9 抑制剂,文献报道的合成路线一共有八步(图4a),而且其中七步都需要快速柱色谱(FCC)分离,总产率1.01%,不适合批量生产。SYNTHIA™则提出了一种新的、更短的路线(图4b),从芳基胺1、醛2和硝基烷烃3的简洁的三组分Aza-Henry反应开始,该反应得到化合物4及其非对映体,产率为78%,顺式:反式分布为12:82,经过水解环合,然后以69%的产率将中间体6磺酰化,并且通过手性色谱以40%的产率分离所需的对映体8,总产率8.83%。总的来说,SYNTHIA™的路线与已知路线相比,步骤数减少3步、产率提高超过八倍,而且减少了合成过程中分离纯化步骤,更适合批量生产。

图4:BRD7/9 抑制剂合成路线优化a)已报道合成路线;b)SYNTHIA™设计的合成路线
2、全新分子α-羟基依替唑仑的合成路线设计与实验验证
第二个分子是α-羟基依替唑仑,是由于治疗焦虑、紧张、抑郁、失眠等疾病的临床用药依替唑仑的代谢产物之一,目前没有合成路线报道。尽管苯并二氮卓类药物的合成方法已经很好地建立,但合成羟基代谢产物依然具有挑战性。利用SYNTHIA™能够设计出非常合理的合成路线并经过了实验的验证(图5)。首先,通过对可购原料9进行氰基取代得到的中间体10,与原料11和S8发生在多组分的Gewald反应,非常巧妙的合成出了氨基噻吩中间体,且带有特定的侧链,并且该步骤路线的设计也识别到了原料11中需要保护的羟基并保护起来。得到的关键中间体12。其余步骤遵循经典的苯二氮卓类转化,以3.2%的总产率得到所需的a-羟基依替唑仑14。

图5:α-羟基依替唑仑合成路线设计与验证
3、其余分子SYNTHIA™设计的合成路线与实验验证
除了上诉的两个分子以外,SYNTHIA™还进行了其它六个分子的合成路线设计和实验结果的验证(图6)。

图6:SYNTHIA™设计的合成路线与实验验证结果.a) ATR抑制剂合成路线优化;b) AML cells抑制剂工艺路线优化;c)(S)-4-Hydroxyduloxetine分子的稳定合成路线设计;d) 5β/6β-Hydroxy-Lurasidone合成路线规避和工艺优化;e)抗心绞痛药物决奈达隆的合成路线规避;f) 全新天然产物 Engelheptanoxide C的合成路线设计与验证
三、总结
SYNTHIA™历经19年的不断迭代更新,利用由有机化学专家和计算机科学家共同手动编码100,000+化学反应规则设计出合理的化合物合成路线。可应用与于复杂化合物、天然产物和全新药物分子的合成路线快速设计;已知化合物的合成工艺路线优化。路线设计时能够考虑到兼顾不兼容基团、基团保护与脱保护、区域和立体选择性、空间位阻和电子效应等因素。越来越多的事实也证明了SYNTHIA™设计出的合成路线的合理性。通过使用SYNTHIA™可以加速分子合成路线的设计,大幅提高实验室合成的效率,加快药物研发的进程。
参考文献:
[1] Klucznik T , Mikulak-Klucznik B , Mccormack M P , et al. Efficient Syntheses of Diverse, Medicinally Relevant Targets Planned by Computer and Executed in the Laboratory.Chem, 2018, 4, 522-532



